Deber de quimica
Anuncio
Mariachi tabasco.. Yamalo lla!!! y contratos al 0991556517
según mi criterio son mas abundantes porque tienen mas tipos de nelaces y este forma parte de diversas composiciones
Aunque puede fabricarse carbono completamente amorfo, el carbono amorfo natural (como el hollín) realmente contiene cristales microscópicos de grafito, algunas veces diamante. A escala macroscópica, el carbono amorfo no tiene una estructura definida, puesto que consiste en pequeños cristales irregulares, pero a escala nanomicroscópica, puede verse que está hecho de átomos de carbono colocados regularmente.
La línea que divide las moléculas orgánicas de las inorgánicos ha originado polémicas e históricamente ha sido arbitraria, pero generalmente, los compuestos orgánicos tienen carbono con enlaces de hidrógeno, y los compuestos inorgánicos, no. Así el ácido carbónico es inorgánico, mientras que el ácido fórmico, el primer ácido graso, es orgánico. El anhídrido carbónico y el monóxido de carbono, son compuestos inorgánicos. Por lo tanto, todas las moléculas orgánicas contienen carbono, pero no todas las moléculas que contienen carbono, son moléculas orgánicas.La etimología de la palabra «orgánico» significa que procede de órganos, relacionado con la vida; en oposición a «inorgánico», que sería el calificativo asignado a todo lo que carece de vida. Se les dio el nombre de orgánicos en el siglo XIX, por la creencia de que sólo podrían ser sintetizados por organismos vivos. La teoría de que los compuestos orgánicos eran fundamentalmente diferentes de los "inorgánicos", fue refutada con la síntesis de la urea, un compuesto "orgánico" por definición ya que se encuentra en la orina de organismos vivos, síntesis realizada a partir de cianato de potasio y sulfato de amonio por Friedrich Wöhler (síntesis de Wöhler). Los compuestos del carbono que todavía se consideran inorgánicos son los que ya lo eran antes del tiempo de Wöhler; es decir, los que se encontraron a partir de fuentes sin vida, "inorgánicas", tales como minerales. El carbono es bien adecuado para este papel central, por el hecho de que es el átomo más liviano capaz de formar múltiples enlaces covalentes. A raíz de esta capacidad, el carbono puede combinarse con otros átomos de carbono y con átomos distintos para formar una gran variedad de cadenas fuertes y estables y de compuestos con forma de anillo. Las moléculas orgánicas derivan sus configuraciones tridimensionales primordialmente de sus esqueletos de carbono. Sin embargo, muchas de sus propiedades específicas dependen de grupos funcionales. Una característica general de todos los compuestos orgánicos es que liberan energía cuando se oxidan.
En los organismos se encuentran cuatro tipos diferentes de moléculas orgánicas en gran cantidad: carbohidratos, lípidos, proteínas y nucleótidos. Todas estas moléculas contienen carbono, hidrógeno y oxígeno. Además, las proteínas contienen nitrógeno y azufre, y los nucleótidos, así como algunos lípidos, contienen nitrógeno y fósforo.
Los carbohidratos son la fuente primaria de energía química para los sistemas vivos. Los más simples son los monosacáridos ("azúcares simples"). Los monosacáridos pueden combinarse para formar disacáridos ("dos azúcares") y polisacáridos (cadenas de muchos monosacáridos).
Los lípidos son moléculas hidrofóbicas que, como los carbohidratos, almacenan energía y son importantes compuestos. La mayoría de los compuestos orgánicos puros se producen hoy de forma artificial, aunque un subconjunto importante todavía se extrae de fuentes naturales porque sería demasiado costosa su síntesis en laboratorio. Los ejemplos incluyen la mayoría de las azúcares, algunos alcaloides, ciertos alimentos tales como la vitamina B12, y en el general, aquellos productos naturales con las moléculas grandes o complicadas que están presentes en concentraciones razonables en organismos vivos.
El análisis estadístico de estructuras químicas se llama informática química. La base de datos de Beilstein contiene una amplia colección de compuestos orgánicos. Un estudio informático que implicaba 5,9 millones de sustancias y 6,5 millones de reacciones, demostró que el universo de compuestos orgánicos consiste en una base de alrededor de 200.000 moléculas muy relacionadas entre sí y de una periferia grande (3,6 millones de moléculas) a su alrededor.[2] La base y la periferia están rodeadas por un grupo de pequeñas islas no-conectadas que contienen 1,2 millones de moléculas, un modelo semejante al www.
Más estadísticas:
Las moléculas de la base (solamente 3,5% del total) están implicadas en el 35% de todas las reacciones que dan lugar al 60% de todas las moléculas.
La distancia media entre dos moléculas en la base es de 8,4 pasos sintéticos, y el 95% de todas las reacciones conectan con menos de 15 pasos. Cualquier molécula de la periferia puede ser alcanzada por una de la base en menos de 3 pasos.
La base contiene el 70% de los 200 productos químicos industriales más utilizados.
Un inventario químico optimo de 300 productos químicos que contenga 10 reactivos de Wittig, 6 reactivos de Grignard, 2 bloques de DNA y 18 aldehidos aromáticos, permite a una compañía química hipotética la síntesis de hasta 1,2 millones de compuestos orgánicos.
Se ha dicho que es suficiente reconocer cerca de 30 moléculas para tener un conocimiento que permita trabajar con la bioquímica de las células. Dos de esas moléculas son los azúcares glucosa y ribosa; otra, un lípido; otras veinte, los aminoácidos biológicamente importantes; y cinco las bases nitrogenadas, moléculas que contienen nitrógeno y son constituyentes claves de los nucleótidos.
17. Enlista los grupos funcionales de los
compuestos orgánicos.
18. De las siguientes moléculas identifica y
enumera la cadena más larga de carbonos.
En cada caso responde: cuántos
carbonos tiene la cadena más larga y
qué tipo de carbonos son.
—¿Qué tipo de enlace covalente puede
formar el carbono?
Mariachi tabasco.. Yamalo lla!!! y contratos al 0991556517
Ahora sin quimia estas son las actividades de las pagina 32 y 33
1. Escribe tres diferencias entre compuestos
orgánicos y compuestos inorgánicos.
orgánicos y compuestos inorgánicos.
COMPUESTOS INORGÁNICOS:
- Sus moléculas pueden contener átomos de cualquier elemento, incluso carbono bajo la forma de CO, CO2, carbonatos y bicarbonatos.
- Se conocen aproximadamente unos 500000 compuestos.
- Son, en general, "termo estables" es decir: resisten la acción del calor, y solo se descomponen a temperaturas superiores a los 700ºC.
- Tienen puntos de ebullición y de fusión elevados.
- Muchos son solubles en H2O y en disolventes polares.
- Fundidos o en solución son buenos conductores de la corriente eléctrica: son "electrólitos".
- Las reacciones que originan son generalmente instantáneas, mediante reacciones sencillas e iónicas.
- Sus moléculas contienen fundamentalmente átomos de C, H, O, N, y en pequeñas proporciones, S, P, halógenos y otros elementos.
- El número de compuestos conocidos supera los 10 millones, y son de gran complejidad debido al número de átomos que forman la molécula.
- Son "termolábiles", resisten poco la acción del calor y descomponen bajo de los 300ºC. suelen quemar facilmente, originando CO2 y H2O.
- Debido a la atracción débil entre las moléculas, tienen puntos de fusión y ebullición bajos.
- La mayoría no son solubles en H2O (solo lo son algunos compuestos que tienen hasta 4 ó 5 átomos de C). Son solubles en disolventes orgánicos: alcohol, éter, cloroformo, benceno.
- No son electrólitos.
- Reaccionan lentamente y complejamente.
2. Razona: ¿por qué el gas propano no es
soluble en agua?
soluble en agua?
Porque el propano esta formado por carbono e hidrogeno(C3H8), y las moleculas de propano se mantienen unidas por fuerzas intermoleculares APOLARES. En cambio, las moleculas de H2O interactuan por fuerzas POLARES.
3. Enlista cinco ejemplos de compuestos
orgánicos y cinco de compuestos inorgánicos.
orgánicos y cinco de compuestos inorgánicos.
ORGANICOS.
Glucosa, Fructosa, Sacarosa, Alcohol Etìlico, Acido Lactico, Acido Acètico, Acetona, Formol, Nitroglicerina, Benzocaina
INORGANICOS,
Cloruro de Sodio, Acido Sulfùrico, Acido Muriàtico, Acido Clorhidrico, Yoduro de Potasio, Oxido de Fierro, Nitrato de Calcio, Dicromato de Potasio, Ac Arsènico, Hidroxido de Aluminio, Cianuro de Potasio, Nitrato de Amonio. Bicarbonato Sòdico, H2O, Diòxido de Carbono, Monoxido de Carbono
Glucosa, Fructosa, Sacarosa, Alcohol Etìlico, Acido Lactico, Acido Acètico, Acetona, Formol, Nitroglicerina, Benzocaina
INORGANICOS,
Cloruro de Sodio, Acido Sulfùrico, Acido Muriàtico, Acido Clorhidrico, Yoduro de Potasio, Oxido de Fierro, Nitrato de Calcio, Dicromato de Potasio, Ac Arsènico, Hidroxido de Aluminio, Cianuro de Potasio, Nitrato de Amonio. Bicarbonato Sòdico, H2O, Diòxido de Carbono, Monoxido de Carbono
4. ¿Por qué los compuestos orgánicos son
más abundantes que los compuestos
inorgánicos?
más abundantes que los compuestos
inorgánicos?
5. ¿En qué formas se encuentra el carbono
en la naturaleza?
en la naturaleza?
R/ El carbono se presenta en la naturaleza en 5 formas alotrópicas que son el diamante , grafito , ulerenos , nanatubos , nanoespumas. El carbono es un elemento químico de número atómico 6 y símbolo C. Es sólido a temperatura ambiente. Dependiendo de las condiciones de formación, puede encontrarse en la naturaleza en distintas formas alotrópicas, carbono amorfo y cristalino en forma de grafito o diamante. Es el pilar básico de la química orgánica; se conocen cerca de 10 millones de compuestos de carbono, y forma parte de todos los seres vivos conocidos.es un elemento ampliamente distribuido en la naturaleza, aunque sólo constituye un 0,025% de la corteza terrestre, donde existe principalmente en forma de carbonatos. El dióxido de carbono es un componente importante de la atmósfera y la principal fuente de carbono que se incorpora a la materia viva. Por medio de la fotosíntesis, los vegetales convierten el dióxido de carbono en compuestos orgánicos de carbono, que posteriormente son consumidos por otros organismos
6. ¿Cómo se define al carbono amorfo?
El carbono amorfo es el carbono que no tiene una estructura cristalina. Como con todos los materiales vítreos, puede presentarse algún orden de corto alcance, pero no hay patrones de largo alcance de las posiciones atómicas.
Aunque puede fabricarse carbono completamente amorfo, el carbono amorfo natural (como el hollín) realmente contiene cristales microscópicos de grafito, algunas veces diamante. A escala macroscópica, el carbono amorfo no tiene una estructura definida, puesto que consiste en pequeños cristales irregulares, pero a escala nanomicroscópica, puede verse que está hecho de átomos de carbono colocados regularmente.
7.¿Cuáles son sus principales usos?
El carbono se encuentra libre en la naturaleza, por tanto su forma alotrópica da para bastante; por ejemplo con el adecuado tratamiento puede convertirse en diamante, respetando las presiones, cortes, transformaciones, temperaturas y reacciones.
Otro uso es el carbón vegetal que usamos para prender calderas. También se emplea en la construcción de la fibra de carbono que es altamente cotizada entre otras para el área militar de alta tecnología, como en los aviones cazabombarderos, ya que es muy útil al proporcionar un chasis que alía muy bien con otros materiales de gran dureza.
También en la pintura el grafito es utilizado.
Asimismo el carbón tiene usos en la purificación de sustancias o refinados químicos, en reactores nucleares, etc..
Otro uso es el carbón vegetal que usamos para prender calderas. También se emplea en la construcción de la fibra de carbono que es altamente cotizada entre otras para el área militar de alta tecnología, como en los aviones cazabombarderos, ya que es muy útil al proporcionar un chasis que alía muy bien con otros materiales de gran dureza.
También en la pintura el grafito es utilizado.
Asimismo el carbón tiene usos en la purificación de sustancias o refinados químicos, en reactores nucleares, etc..
8. escicirbe en la imagen del ciclo del carbono
nota esta imagen es solo un modelo de como hacer
nota esta imagen es solo un modelo de como hacer
9. Enlista cuatro compuestos del carbono,
naturales y sintéticos, de uso en la
vida cotidiana.
naturales y sintéticos, de uso en la
vida cotidiana.
Los compuestos orgánicos son sustancias químicas basadas en cadenas de carbono e hidrógeno. En muchos casos contienen oxígeno, y también nitrógeno, azufre, fósforo, boro y halógenos. No son moléculas orgánicas los carburos, los carbonatos y los óxidos de carbono.
Moléculas orgánicas naturales: Son las sintetizadas por los seres vivos, y se llaman biomoléculas, las cuales son estudiadas por la bioquímica.
Moléculas orgánicas artificiales o sinteticos: Son sustancias que no existen en la naturaleza y han sido fabricadas por el hombre como los plásticos.
La línea que divide las moléculas orgánicas de las inorgánicos ha originado polémicas e históricamente ha sido arbitraria, pero generalmente, los compuestos orgánicos tienen carbono con enlaces de hidrógeno, y los compuestos inorgánicos, no. Así el ácido carbónico es inorgánico, mientras que el ácido fórmico, el primer ácido graso, es orgánico. El anhídrido carbónico y el monóxido de carbono, son compuestos inorgánicos. Por lo tanto, todas las moléculas orgánicas contienen carbono, pero no todas las moléculas que contienen carbono, son moléculas orgánicas.La etimología de la palabra «orgánico» significa que procede de órganos, relacionado con la vida; en oposición a «inorgánico», que sería el calificativo asignado a todo lo que carece de vida. Se les dio el nombre de orgánicos en el siglo XIX, por la creencia de que sólo podrían ser sintetizados por organismos vivos. La teoría de que los compuestos orgánicos eran fundamentalmente diferentes de los "inorgánicos", fue refutada con la síntesis de la urea, un compuesto "orgánico" por definición ya que se encuentra en la orina de organismos vivos, síntesis realizada a partir de cianato de potasio y sulfato de amonio por Friedrich Wöhler (síntesis de Wöhler). Los compuestos del carbono que todavía se consideran inorgánicos son los que ya lo eran antes del tiempo de Wöhler; es decir, los que se encontraron a partir de fuentes sin vida, "inorgánicas", tales como minerales. El carbono es bien adecuado para este papel central, por el hecho de que es el átomo más liviano capaz de formar múltiples enlaces covalentes. A raíz de esta capacidad, el carbono puede combinarse con otros átomos de carbono y con átomos distintos para formar una gran variedad de cadenas fuertes y estables y de compuestos con forma de anillo. Las moléculas orgánicas derivan sus configuraciones tridimensionales primordialmente de sus esqueletos de carbono. Sin embargo, muchas de sus propiedades específicas dependen de grupos funcionales. Una característica general de todos los compuestos orgánicos es que liberan energía cuando se oxidan.
En los organismos se encuentran cuatro tipos diferentes de moléculas orgánicas en gran cantidad: carbohidratos, lípidos, proteínas y nucleótidos. Todas estas moléculas contienen carbono, hidrógeno y oxígeno. Además, las proteínas contienen nitrógeno y azufre, y los nucleótidos, así como algunos lípidos, contienen nitrógeno y fósforo.
Los carbohidratos son la fuente primaria de energía química para los sistemas vivos. Los más simples son los monosacáridos ("azúcares simples"). Los monosacáridos pueden combinarse para formar disacáridos ("dos azúcares") y polisacáridos (cadenas de muchos monosacáridos).
Los lípidos son moléculas hidrofóbicas que, como los carbohidratos, almacenan energía y son importantes compuestos. La mayoría de los compuestos orgánicos puros se producen hoy de forma artificial, aunque un subconjunto importante todavía se extrae de fuentes naturales porque sería demasiado costosa su síntesis en laboratorio. Los ejemplos incluyen la mayoría de las azúcares, algunos alcaloides, ciertos alimentos tales como la vitamina B12, y en el general, aquellos productos naturales con las moléculas grandes o complicadas que están presentes en concentraciones razonables en organismos vivos.
El análisis estadístico de estructuras químicas se llama informática química. La base de datos de Beilstein contiene una amplia colección de compuestos orgánicos. Un estudio informático que implicaba 5,9 millones de sustancias y 6,5 millones de reacciones, demostró que el universo de compuestos orgánicos consiste en una base de alrededor de 200.000 moléculas muy relacionadas entre sí y de una periferia grande (3,6 millones de moléculas) a su alrededor.[2] La base y la periferia están rodeadas por un grupo de pequeñas islas no-conectadas que contienen 1,2 millones de moléculas, un modelo semejante al www.
Más estadísticas:
Las moléculas de la base (solamente 3,5% del total) están implicadas en el 35% de todas las reacciones que dan lugar al 60% de todas las moléculas.
La distancia media entre dos moléculas en la base es de 8,4 pasos sintéticos, y el 95% de todas las reacciones conectan con menos de 15 pasos. Cualquier molécula de la periferia puede ser alcanzada por una de la base en menos de 3 pasos.
La base contiene el 70% de los 200 productos químicos industriales más utilizados.
Un inventario químico optimo de 300 productos químicos que contenga 10 reactivos de Wittig, 6 reactivos de Grignard, 2 bloques de DNA y 18 aldehidos aromáticos, permite a una compañía química hipotética la síntesis de hasta 1,2 millones de compuestos orgánicos.
Se ha dicho que es suficiente reconocer cerca de 30 moléculas para tener un conocimiento que permita trabajar con la bioquímica de las células. Dos de esas moléculas son los azúcares glucosa y ribosa; otra, un lípido; otras veinte, los aminoácidos biológicamente importantes; y cinco las bases nitrogenadas, moléculas que contienen nitrógeno y son constituyentes claves de los nucleótidos.
10. Escribe tres nombres de medicamentos
que contengan compuestos orgánicos
y escribe la fórmula del principal ingrediente
activo.
que contengan compuestos orgánicos
y escribe la fórmula del principal ingrediente
activo.
11.- ¿Por qué el carbono es tan importante
para la vida?
para la vida?
El carbón es un combustible fósil más abundante (las reservas de carbón son extensas y están presentes en muchos países), seguro (el carbón es estable y por tanto es el combustible fósil más seguro desde los puntos de vista de su transporte, almacenamiento y utilización) y de suministro garantizado en el mundo (la abundancia de las reservas significa se puede garantizar el suministro del recurso y ello a su vez, a precios).
12.- ¿Que es hibridación?
En química, se conoce como hibridación a la interacción de orbitales atómicos dentro de un átomo para formar nuevos orbitales híbridos. Los orbitales atómicos híbridos son los que se superponen en la formación de los enlaces, dentro de la teoría del enlace de valencia, y justifican la geometría molecular.
13.- ¿Cuántos tipos de hibridación existen
para el carbono?
para el carbono?
14. Dibuja las geometrías de los tipos de hibridación
del carbono.
del carbono.
Esta en l aanterior
15.- ¿Qué es un enlace covalente?
Principalmente los compuestos orgánicos tienen enlaces covalentes, los cuales se producen
por compartición de pares de electrones.
por compartición de pares de electrones.
16.-¿En qué tipo de cadenas se puede encontrar,
agrupados, a los compuestos
con carbono?
agrupados, a los compuestos
con carbono?
Cada átomo de carbono puede unirse a tantos elementos como enlaces libres posea. Las
cadenas carbonadas pueden ser abiertas o cerradas; las abiertas pueden ser ramificadas
y las cerradas o ciclos también pueden tener sustituyentes.
cadenas carbonadas pueden ser abiertas o cerradas; las abiertas pueden ser ramificadas
y las cerradas o ciclos también pueden tener sustituyentes.
17. Enlista los grupos funcionales de los
compuestos orgánicos.
18. De las siguientes moléculas identifica y
enumera la cadena más larga de carbonos.
En cada caso responde: cuántos
carbonos tiene la cadena más larga y
qué tipo de carbonos son.
—¿Qué tipo de enlace covalente puede
formar el carbono?
19. Escribe:
a. La masa atómica del carbono.
a. La masa atómica del carbono.
número másico
A = 12.
b. Posición del carbono en la tabla
periódica.
A = 12.
b. Posición del carbono en la tabla
periódica.
El carbono tiene número atómico Z = 6 y
20. Dibuja el átomo de carbono.
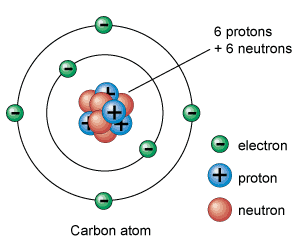
21. Escribe tres propiedades de los compuestos
orgánicos.
20. Dibuja el átomo de carbono.

21. Escribe tres propiedades de los compuestos
orgánicos.
Están formados principalmente por carbono (C), hidrógeno (H), oxígeno (O), nitrógeno
(N), fósforo (P), azufre (S), flúor (F), cloro (Cl), bromo (Br), yodo (I), entre otros elementos.
• Siempre contienen elementos que contienen al carbono, que a su vez, pueden unirse
entre sí.
• Sus reacciones son lentas y complejas.
• Son inestables al calor.
• Son insolubles en agua.
• Son solubles en contacto con solventes no polares.
• Los compuestos generalmente tienen pesos moleculares altos.
• No conducen corriente eléctrica debido a que no se ionizan.
• Sus puntos de ebullición y de fusión son bajos
• Generalmente contienen enlaces covalentes
22. ¿Cómo se definen a los hidrocarburos?
(N), fósforo (P), azufre (S), flúor (F), cloro (Cl), bromo (Br), yodo (I), entre otros elementos.
• Siempre contienen elementos que contienen al carbono, que a su vez, pueden unirse
entre sí.
• Sus reacciones son lentas y complejas.
• Son inestables al calor.
• Son insolubles en agua.
• Son solubles en contacto con solventes no polares.
• Los compuestos generalmente tienen pesos moleculares altos.
• No conducen corriente eléctrica debido a que no se ionizan.
• Sus puntos de ebullición y de fusión son bajos
• Generalmente contienen enlaces covalentes
22. ¿Cómo se definen a los hidrocarburos?
son comouestos organicos en la tierra. Formando unciamente por atomos de carbono e jidrogeno. La esteuxtura molecular consiste en un armazon de carbono y atomos de hifrogeno
23. Realiza un esquema de los hidrocarburos
y sus ramificaciones.
23. Realiza un esquema de los hidrocarburos
y sus ramificaciones.






Gracias mijin estoy me sirvio bastante para acabr de aser este trabajo felicidades y espero que sigas ayudando a muchas personas mas
ResponderEliminar:)
Este comentario ha sido eliminado por el autor.
EliminarMuchas gracias, de verdad acabas de salvar a un individuo. Pero... Y la 18?
ResponderEliminarfalto la 18 bro :( pero de igual gracias, no todos los héroes llevan capa :V
ResponderEliminarBaya que bien servicio :v
ResponderEliminarSolo nesesitaba la 18 y no esta que mal. Solo esta la pregunta pero no la respuesta
ResponderEliminarExcelente servicio
ResponderEliminar